イオンとはどんなものなのか?
プラズマとはどんな状態なのか?
素粒子には、どんな物があるのかについて説明します。
イオンの状態とは
イオンとプラズマの状態に、影響をあたえるものは電子の状態です。
★ 通常の状態の原子は、図のように原子核のプラスと電子のマイナスが打ち消しあって 電気的には中性 の状態になっています。
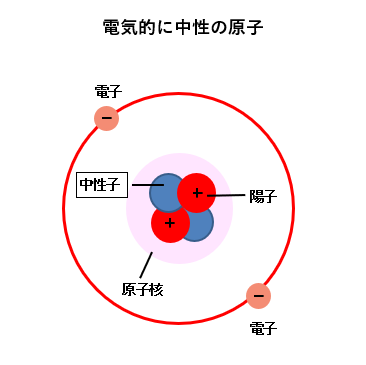
★ しかし、図のように、原子に外部から何らかの刺激が与えられると、そのエネルギーによって電子が外に 放出されたり、受け取ったり することがあります。
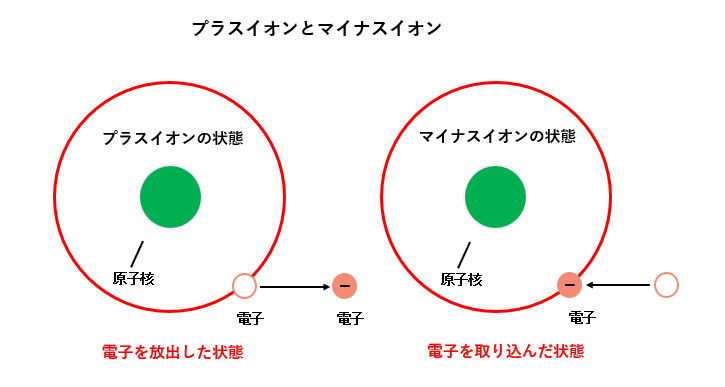
★ このようになると、いままで電気的には中性だった原子から
マイナスである電子が飛び出したので プラス を帯びた状態になります。
反対に、電子を取り込んだ原子は マイナス を帯びた状態になります。
このような、原子の状態のことを イオン と呼びます。
したがって、イオンにはプラスの電荷をもつ プラスイオン と
マイナスの電荷をもつ マイナスイオン があります。
イオンという呼び方は、マイケル・ファラデー(1791年9月22日 – 1867年8月25日)イギリスの化学者・物理学者によってつけられました。
■ ナトリウムイオン
ナトリウムは原子番号が11の元素です。
M殻にある電子が、何らかのエネルギーを受けて飛び出すと 陽イオン となり
安定した ナトリウムイオン となります。
■ 塩素イオン
塩素は原子番号が17の元素です。
M殻に外から電子をもらうと 陰イオン なり、塩素イオン となります。
■ イオン化傾向
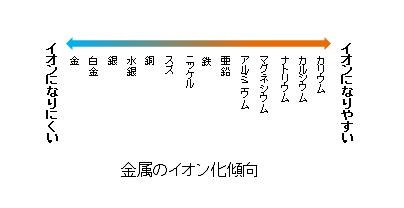
★ 電子が移動すると電流が流れるのですが
電荷を帯びている原子や分子(つまりイオンの状態) が移動しても電流が流れることになります。
水の入った容器に電線を入れて電気を通すとき
そのままでは電流が流れなくても、食塩を入れて 食塩水 にすると電流が流れます。
これは食塩が水に溶けたときに、食塩(NaCl)が
ナトリウムイオンと塩素イオン に分かれることで、電気を通しやすくなったためです。
イオンを使った技術は、電池(リチウムイオン電池など)
電気透析(脱塩・殺菌)、バイオ技術などに使われています。
プラズマとは
プラズマ状態は図のように気体分子の状態で
原子核と電子がバラバラになって動いている状態のことを プラズマ状態 といいます。
- 気体分子がプラス電荷をもっているイオンとマイナス電荷をもつ電子に分離(電離)している。
- それぞれが別々に動いていて、しかも全体としては電気的に中性になっている。
- プラスイオンと電子が混合している気体を プラズマ とよびます。

★ プラズマを作るには期待を数万度C以上の超高温にすることで作る場合と
気体に高電圧をかけることで作る場合があります。
北極などで観測されるオーロラは
太陽から放射されたプラズマ粒子(太陽風)に
大気中の酸素や窒素の粒子と衝突して起こるものです。
プラズマを使った技術は、蛍光灯、アーク溶接器、プラズマカッター、プラズマディスプレイ
などに使われています。
素粒子とは何か
物質をどんどん小さくしていった時に、最後にたどりつくものが素粒子です。
すべての物質は分子と原子でできています。
原子は原子核と原子核を取り巻く電子でできています。
そして、原子核は陽子や中性子でできています。
さらに陽子や中性子は3個のクォークで構成されていることが知られています。
素粒子は大きく3つに分けることができます
素粒子
- 物質を作る素粒子-「フェルミ粒子」
- 力を伝える素粒子 -「ゲージ粒子」
- 質量を与える素粒子 -「ヒッグス粒子」
素粒子のフェルミ粒子はクオークとレプトンのグループに分かれる
素粒子クオークのグループ
- アップとダウン
- チャームとストレンジ
- トップとボトムがありそれぞれが対になっています。
素粒子レプトンのグループ
- 電子と電子ニュートリノ
- ミューとミューニュートリノ
- タウとタウニュートリノがありそれぞれが対になっています。
電子はレプトンに分類される素粒子に入ります。
■ たとえば、ヒトを素粒子に分解してみると
★ ヒト → 細胞 → 分子 → 原子 → 原子核(陽子と中性子)、電子 のようにわけられます。
原子を素粒子の電荷量で見る
素粒子アップクオークの持つ電荷は \(\cfrac{2}{3e}\) クーロンであり
素粒子ダウンクオークの持つ電荷は \(-\cfrac{1}{3e}\) クーロンとされています。
■ 陽子の電荷量
素粒子アップクオーク2つと素粒子ダウンウオーク1つでできています。
電荷的には次のようになります。
陽子の電荷量\(=\cfrac{2}{3}e×2+\left(-\frac{1}{3}e \right)=e\) [C]
■ 中性子はクオーク族
アップクオーク1つとダウンウオーク2つでできています。
電荷的には次のようになります。
中性子の電荷量\(=\cfrac{2}{3}e+\left(-\frac{1}{3}e×2 \right)=0\) [C]
■ 電子の持つ電荷は -e [C]
従って原子を電荷量で見ると、陽子 \(+e\) 、中性子が \(0\) 、電子 \(-e\) なので合計すると電気的に0(ゼロ)になります。
原子は原子番号=陽子の数=電子の数となっています。
以上で「イオン・プラズマ・素粒子について」の説明を終わります。